ACTIVIDAD PARA OCTAVO
- beniredome
- 31 mar 2019
- 2 Min. de lectura
8°
como se nombran los compuestos inorgánicos
Conceptos claves:
Nomenclatura: es la forma de nombrar los elementos y compuestos.
Compuestos: son sustancias formadas por átomos de dos o más elementos y pueden clasificarse según los elementos que los constituyen o según los otros compuestos de donde provengan.
Función química: llamamos función química a una serie de sustancias que presentan un conjunto de propiedades comunes y específicas que nos permiten diferenciarlos de los demás. Entre las principales tenemos OXIDOS, HIDROXIDOS, ACIDOS Y SALES.
Grupo funcional: llamamos grupo funcional al átomo o conjunto de átomos presentes en determinados compuestos y le dan características
propias:
Por ejemplo: Ca (OH) Na(OH) CU(OH) Fe(OH) Todos corresponden a la misma función química (los hidróxidoS).

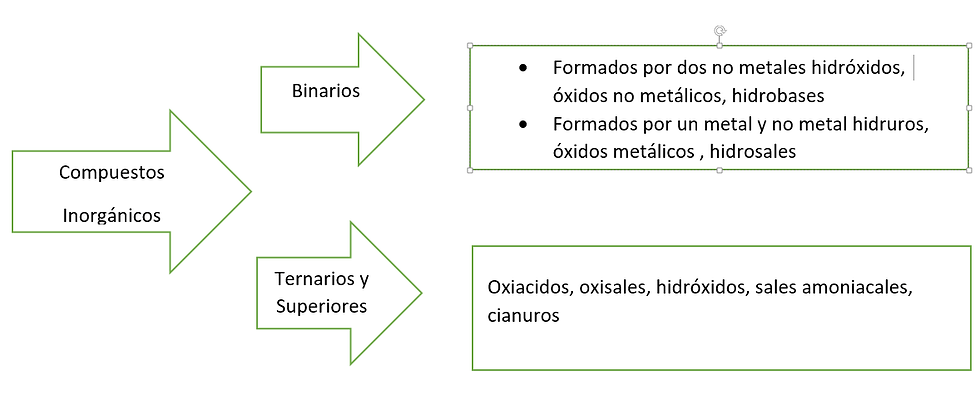
Los compuestos inorgánicos se dividen en binarios (aquellos con dos elementos diferentes). Ternarios y superiores (que tienen tres o más elementos).
Sistema de nomenclatura:
Se utilizan 3 sistemas
1 sistema clásico, tradicional o común : emplea un nombre constituido por dos palabras; la primera corresponde al nombre de la función (o del grupo mas electronegativo)y la segunda al nombre del metal o del ion electropositivo; hace uso además de los siguientes sufijos
Uro: para el primer nombre de los hidruros, hidracidos e hidrosales
Ido: para los óxidos.
Oso :para menor estado de oxidación
Ico: para mayor estado de oxidación
Ito: mayor estado de oxidación
Ato menor estado de oxidación.
Algunas ocaciones se utilizan los prefijos per, hiper, hipo también indican el nero de oxidación de uo de los elementos.
Meta piro y orto para los compuestos oxácidos y oxisales del fosforo arsénico y antimonio.
Ejemplos:
CaCo: carbonato cálcico
HClO: hipoclorito sódico.
2 SISTEMA racional o sistemático
Cuya base es la proporción de los elementos en el compuesto utiliza prefijos numéricos para indicar el numero de cada tipo de átomo que conforman la sustancia.
Prefijos números prefijos números
Mono 1 hexa 6
Di 2 hepta 7
Tri 3 octa 8
Tetra 4 nona 9
Penta 5 deca 10
Ejemplo: CO: MONOXIDO DE CARBONO
FeCl2: dicloruro de hierro
3 Sistema stock- Werner : este utiliza un numero romano entre paréntesis después del del nombre del metal ( o elemento electro positivo) para indicar su numero de oxidaciones elimina las terminaciones oso,ico, e ito y conserva las terminaciones uro para los compuestos binarios de un metal o un no metal con hidrogeno ido para los oxidos y la terminación ato para cualquier clase de compuesto ionico o covalente. Se conservan los prefijos meta piro y orto
Ejemplo NaClO: CLORATO DE SODIO I
CaCO3: : CARBONATO DE CALCIO II
NOMENCLATURA PARA LOS ÓXIDOS: se tienen en cuenta las siguientes reglas:
1si el elemento (metano o no metal) combinado con el oxígeno (O) posee un solo número de oxidación se escribe así : OXIDO+ EL NOMBRE DEL ELEMENTO
2. si el elemento ( metal o no metal )combinado con el oxigeno(O) posee dos numeros de oxidación: OXIDO +ELEMENTO CON LA TERMINACIÓN OSO para el menor numero de oxidación ICO para el mayor numero de oxidación.
3 si el elemento ( metal o no metal) posee tres o mas números de oxidación:
Oxido+hipo +nombre del elemento + oso para el numero mínimo de oxidación
Oxido + elemento Ico para el mayor numero de oxidación
Oxido + per + elemento ico para el mayor (máximo)
Teniendo en cuenta la anterior información nombrar en el cuaderno los siguientes óxidos




Comentarios